
Atome sind definiert als die kleinsten Teilchen jeder Materie und können nicht auf die übliche Weise geteilt werden. Sie bestehen aus einem Kern und einer Hülle, die geladene Teilchen enthält. Der Kern enthältProtonenundNeutronen, während die HülleElektronenenthält. Die Merkmale der Atome hängen von den Eigenschaften der Elemente ab. Um Materie zu bilden, verbinden sich mehrere Atome zu Molekülen, die wiederum Elemente bilden. Die Atome können jedoch nicht einfach nebeneinander sitzen, sondern müssen auf irgendeine Weise miteinander verbunden sein. Dies geschieht durch so genannte Atombindungen. Es gibt mehrere Arten von Atombindungen, die wichtigsten sind ::

metallische Bindungen
Diese Bindungen sind in metallischen Materialien vorhanden. Die Elektronen sind schwach aneinander gebunden, und in einigen Materialien ist es sogar möglich, Elektronen in völlig freiem Zustand zu übertragen, ohne die Struktur zu beschädigen. Hier wirkt eine anziehende Kraft zwischen dem Kern und seiner Hülle. Metalle haben daher in der Regel eine geringe Härte und Festigkeit, Plastizität, Wärme- und elektrische Leitfähigkeit.
Kovalente Bindungen
Diese Bindungen sind die stärksten und beruhen auf der gegenseitigen Aufteilung freier Elektronen zwischen den Atomen eines oder mehrerer Elemente. Stoffe mit solchen Bindungen sind in der Regel sehr stabil, schwer zu schmelzen, haben einen hohen Schmelzpunkt und sind elektrisch und thermisch nicht leitend.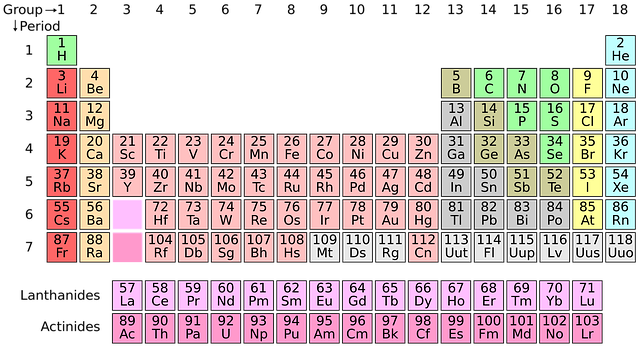
Ionische Bindungen
Ionen sind geladene Teilchen, die positiv oder negativ sein können. Vielleicht hast du schon einmal eine bunte Tabelle gesehen, das Periodensystem der Elemente. Die Elemente auf der linken Seite des Periodensystems (insbesondere die der Gruppen 1 und 2) bilden mit größerer Wahrscheinlichkeit positiv geladene Ionen , die als elektropositivbezeichnet werden. Elemente auf der rechten Seite (sogenannteelektronegative Elemente) nehmen eher Elektronen auf (sogenannteelektronegative Elemente) und tragen eine negative Ladung. Es ist bekannt, dass sich entgegengesetzte Ladungen gegenseitig anziehen, so dass positiv und negativ geladene Ionen zusammenkommen und Ionenbindungen bilden. Diese Bindung findet man in salzartigen Feststoffen (z. B.Natriumchlorid,Calciumfluorid)
. Es gibt noch andere Bindungen zwischen Atomen, die jedoch weniger bedeutend sind. Beispiele hierfür sinddie zwischenmolekularen Van-der-Waals-Kräfte, die am schwächsten sind und z. B. zwischen den Schichten von Graphit auftreten.

